Migotanie przedsionków to najczęstsze zaburzenie rytmu serca. Aktualnie rozpoznaje się je u ok. 400 tys. osób w Polsce, jednak wraz ze starzejącą się populacją, a także aktywnym poszukiwaniem zaburzeń rytmu serca, w ciągu najbliższych lat liczba ta może wzrosnąć nawet 3-krotnie. Co niepokojące, znaczna część pacjentów ze względu na brak objawów i napadowy charakter, może nie być zdiagnozowana i być w ryzyku śmiertelnych powikłań zakrzepowo-zatorowych. Szacuje się, że ok. 20% udarów mózgu ma związek z migotaniem przedsionków, z czego ok. 30 tysięcy z nich kończy się zgonem co w praktyce oznacza, że średnio co 8 minut w Polsce, ktoś umiera, w wyniku udaru mózgu. Jednak udar to nie jedyne powikłanie migotania przedsionków. Wytyczne Europejskiego Towarzystwa Kardiologicznego wskazują na związek z niewydolnością serca, pogorszeniem jakości życia pacjenta, a także depresją. Ponadto u co czwartego pacjenta dotkniętego migotaniem przedsionków można wykazać nieme klinicznie mikroudary mózgu. W literaturze przedmiotu zwrócono uwagę na silny związek pomiędzy migotaniem przedsionków, a występowaniem demencji, a także można znaleźć coraz więcej doniesień opisujących wpływ migotania przedsionków na rozwój mniej nasilonych, ale równie uciążliwych dla pacjenta zaburzeń poznawczych, niezależnych od statusu socjoekonomicznego, ciśnienia tętniczego, frakcji wyrzutowej serca czy też przebytych w przeszłości udarów mózgu.
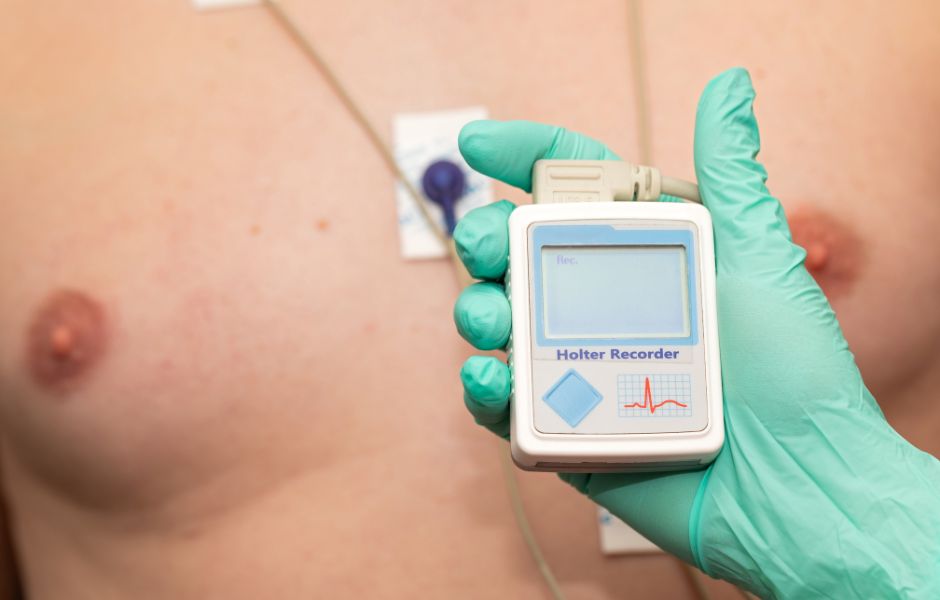
Z tego względu Wytyczne Europejskiego Towarzystwa Kardiologicznego kładą nacisk na badania przesiewowe migotania przedsionków, wskazując na szczególne korzyści w populacji powyżej 65 roku życia i zwracają uwagę na możliwości wykorzystania do tego celu nowoczesnych technologii medycznych takich jak: smartwatch’e, personalne urządzenia EKG, czy aplikacje mobilne, które w większości opierają się o dwie technologie – fotopletyzmografie (PPG) lub elektrokardiografie (EKG).
Złotym standardem w diagnostyce migotania przedsionków jest 24h holter EKG, jednak wiele prac wskazuje, że jego możliwości diagnostyczne są ograniczone, a komfort jego użytkowania dla pacjenta jest niski [3]. Do długoterminowego pomiaru EKG można również zastosować wszczepialne urządzenia pętlowe (ILR), jednak ich wykorzystanie wiąże się z wieloma ograniczeniami takimi jak: inwazyjność, niska dostępność i wysoki koszt. W związku z tym poszukiwane są nowe metody screeningu i diagnostyki migotania przedsionków oparte o zarówno medyczne jak i niemedyczne urządzenia osobiste z funkcją pomiarową. Coraz większą rolę w tym wyścigu zaczynają odgrywać firmy technologiczne, wcześniej nie związane ze światem medycznym takie jak Apple czy Huawei, które funkcja za funkcją i badanie za badaniem zyskują coraz większe zaufanie lekarzy i pacjentów.
Apple Heart Study, przeprowadzone na ponad 400 tysiącach użytkowników wykazało 35% czułość funkcji powiadomień o nieregularnym tętnie, w populacji powyżej 65 roku życia, z czego 89% prawdziwie pozytywnych wyników miało epizody AF trwające co najmniej 1 godzinę.
Wyniki tego badania, mimo wielu kontrowersji i obaw ze strony środowiska wskazują na potencjalne korzyści z sygnalizacji nieregularnego tętna pacjenta w badaniach przesiewowych w populacji powyżej 65 lat, czyli właśnie wtedy, gdy screening jest najbardziej koszto-efektywny. W badaniu Huawei Heart study osiągnięto podobny wynik – 91,6%, gdzie monitorowano PPG przez 60s co 10 minut na przestrzeni dwóch tygodni.
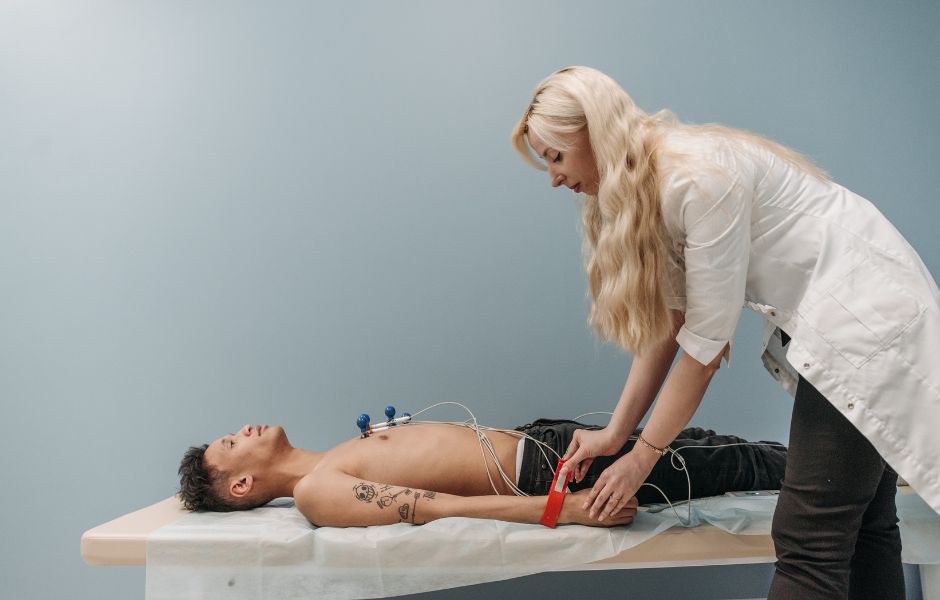
Obecnie według wytycznych do rozpoznania migotania przedsionków konieczny jest zapis o długości nie mniejszej, niż 30 sekund z conajmniej 1-odprowadzeniowego EKG, choć niewykluczone, że w najbliższych latach może się to zmienić i kolejne dowody dadzą lekarzom możliwość postawienia diagnozy na podstawie sygnału optycznego dostarczanego przez popularne i tanie pulsoksymetry czy smartwatch’e lub krótszy sygnał EKG.
W ostatnich latach na popularności zyskują również metody pozwalające na wydłużenie czasu monitorowania pacjenta np. przez wykorzystanie specjalistycznych patch’y [6] lub metoda holtera zdarzeniowego (Event holter), która pozwala na wydłużenie czasu monitorowania pacjenta i opiera się na wykonaniu pomiaru EKG w momencie odczuwania przez pacjenta objawów lub automatycznie, gdy zostaną spełnione określone warunki np. rytm serca osiągnie wartość powyżej określonego progu lub wystąpi potencjalny czynnik wyzwalający migotanie [7]. W badaniach wykazano również, że dodatkowy telemonitoring EKG, polegający na przesyłaniu pomiarów z domu pacjenta z wykorzystaniem sieci telefonicznej lub internetu i bieżącej analizie przez zespół specjalistów zwiększa szansę rozpoznania arytmii oraz skraca czas do postawienia diagnozy, co pozwala na ograniczenie kosztów badania, niezależnie od użytej technologii.
Tego typu telemonitoring EKG jest szczególnie wskazany w diagnostyce migotania przedsionków u pacjentów z wysokim ryzykiem powikłań zakrzepowo-zatorowych wyrażonego w skali CHA2DS2-VASc, u osób po udarze, gdy nie udało się potwierdzić migotania przedsionków standardowymi metodami. Konsensus ekspertów Polskiego Towarzystwa Kardiologicznego wskazuje, że optymalny czas monitorowania powinien wynosić co najmniej 30 dni, jednak warto zwrócić uwagę, że większość istotnych zaburzeń rytmu serca udaje się zdiagnozować już w pierwszym tygodniu.
Mimo obiecujących wyników oraz wielu dostępnych metod nieinwazyjnego screeningu i diagnostyki migotania przedsionków wciąż brakuje optymalnej organizacyjnie i kosztowo, skutecznej metody diagnostycznej, bez znaczącego ograniczenia jakości życia pacjenta, a nowoczesne technologie takie jak smartwatch’e, nowoczesne patch’e czy personalne urządzenia EKG wydają się być „samotnymi wyspami”, bez jasnej ścieżki kontynuacji opieki po rozpoznaniu. Do rozwiązania problemu kluczowa może okazać się kompleksowe podejście i ścisła współpraca twórców technologii z podmiotami leczniczymi, a także płatnikiem i stworzenie pełnej ścieżki opieki nad pacjentem z migotaniem przedsionków.
Literatura
- Stępień A. (ed). Neurologia. Wyd. I. , Warszawa 2014: 171.
- Hindricks G, Potpara T, Dagres N, et al. 2020 ESC Guidelines for the diagnosis and management of atrial fibrillation developed in collaboration with the European Association for Cardio-Thoracic Surgery (EACTS): The Task Force for the diagnosis and management of atrial fibrillation of the European Society of Cardiology (ESC) Developed with the special contribution of the European Heart Rhythm Association (EHRA) of the ESC [published correction appears in Eur Heart J. 2021 Feb 1;42(5):507] [published correction appears in Eur Heart J. 2021 Feb 1;42(5):546-547] [published correction appears in Eur Heart J. 2021 Oct 21;42(40):4194]. Eur Heart J. 2021;42(5):373-498. doi:10.1093/eurheartj/ehaa612
- Hermans ANL, Gawalko M, Pluymaekers NAHA, et al. Long-term intermittent versus short continuous heart rhythm monitoring for the detection of atrial fibrillation recurrences after catheter ablation. Int J Cardiol. 2021;329:105-112. doi:10.1016/j.ijcard.2020.12.077
- Perez MV, Mahaffey KW, Hedlin H, et al. Large-Scale Assessment of a Smartwatch to Identify Atrial Fibrillation. N Engl J Med. 2019;381(20):1909-1917. doi:10.1056/NEJMoa1901183
- Guo, Y. et al. Mobile health technology for atrial fibrillation screening using photoplethysmography-based smart devices: The HUAWEI Heart study, J. Am. Coll. Cardiol. 74, 2365–2375 (2019).
- Barrett PM, Komatireddy R, Haaser S, et al. Comparison of 24-hour Holter monitoring with 14-day novel adhesive patch electrocardiographic monitoring. Am J Med. 2014;127(1):95.e11-95.e9.5E17. doi:10.1016/j.amjmed.2013.10.003
- de Asmundis C, Conte G, Sieira J, et al. Comparison of the patient-activated event recording system vs. traditional 24 h Holter electrocardiography in individuals with paroxysmal palpitations or dizziness. Europace. 2014;16(8):1231-1235. doi:10.1093/europace/eut411
- Piotrowicz R, Krzesiński P, Balsam P, et al. Rozwiązania telemedyczne w kardiologii — opinia ekspertów Komisji Informatyki i Telemedycyny Polskiego Towarzystwa Kardiologicznego, Sekcji Elektrokardiologii Nieinwazyjnej i Telemedycyny Polskiego Towarzystwa Kardiologicznego oraz Komitetu Nauk Klinicznych Polskiej Akademii Nauk. Kardiol Pol. 2018; 76(3): 698–707, doi: 10.5603/KP.a2018.0058.




